Sorunun çözümüne başlayacak olursak öncelikle kömürün tanımını inceleyim.
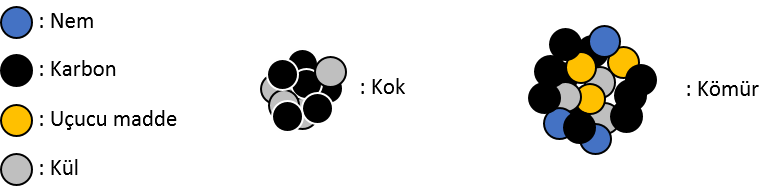
İlk olarak kömür numunesi etüvde 105 °C sıcaklıkta kurutulmaktadır. Aşağıdaki şekilde süreç özetlenmeye çalışılmıştır. Numune
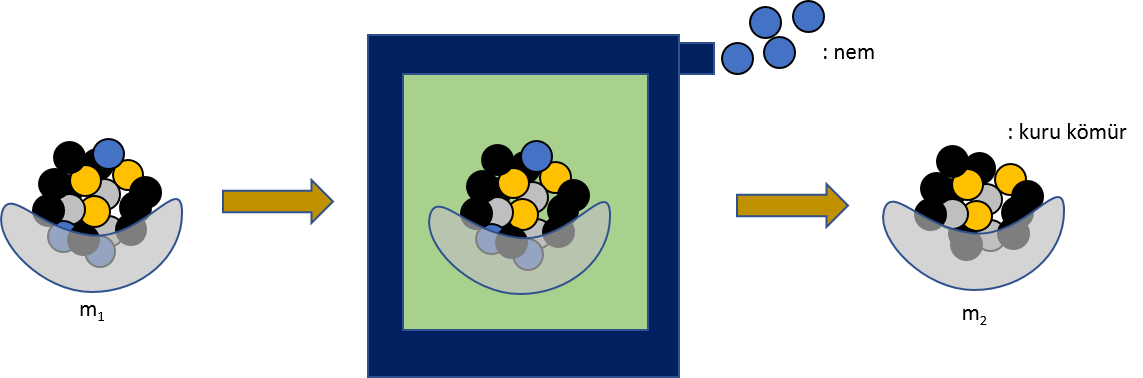
\[ Yüzde \ nem= { (m_1 - m_2) \over m_1} \times 100\]
\[ Yüzde \ nem= { (2,235 - 2,112 \ g) \over 2,235 \ g} \times 100=5,50\]
Daha sonra numune kapağı kapalı bir krozeye yerleştirilerek kül fırınında 950 ° sıcaklıkta ısıtılıyor. İçeriye oksijen girmediğininde yanma gerçekleşmeyecektir ancak kinetik enerjileri artan organik uçucu bileşenler krozeden dışarı sızacaktır.

Uçucu madde analizi de aşağıdaki şekilde hesaplanacaktır. Görüldüğü gibi uçucu maddenin uzaklaşmasından sonra krozede kok (m5) kalmaktadır.
\[ m_{kuru \ numune}= m_4- m_{3} = 22,2285-21,1345 g=1,094 \ g\]
\[ m_{kok}= m_{5} - m_{3}= 21,9112-21,1345 g=0,7767 \ g\]
\[ Yüzde \ kok= { m_{kok} \over m_{kuru \ numune}} \times 100\]
\[ Yüzde \ kok= { 0,7767 \over 1,094} \times 100=71,0\]
\[ m_{uçucu \ madde}= m_{kuru \ numune} - m_{kok}= 1,094-0,7767 g=0,3173 \ g\]
\[ Yüzde \ uçucu \ madde= { m_{uçucu \ madde} \over m_{kuru \ numune}} \times 100\]
\[ Yüzde \ uçucu \ madde= { 0,3173 \ g \over 1,094 \ g} \times 100=29,0\]
Kok sabit karbon ve külden oluştuğundan numune fırında yakıldığında içeriğindeki karbon karbondioksit vermek üzere uzaklaşacak ve kül kalacaktır.
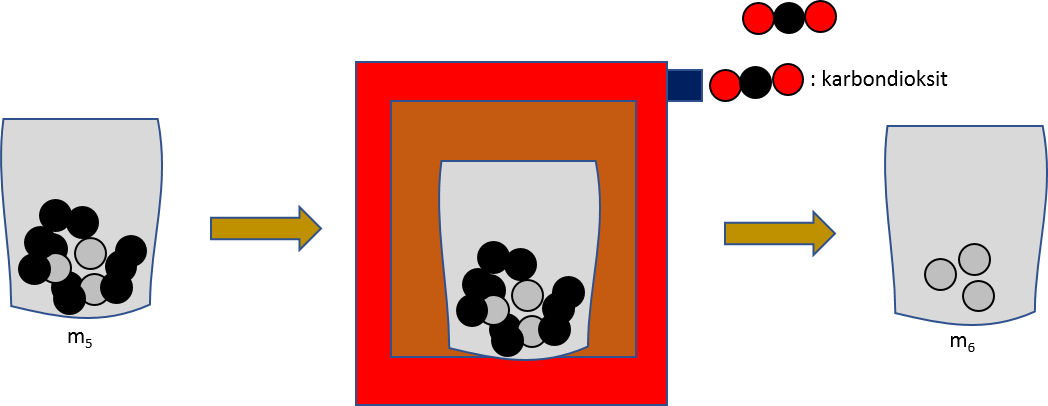
\[ m_{kül}= m_{6} - m_{3}= 21,2351-21,1345 g=0,1006 \ g\]
\[ Yüzde \ kül= { m_{kül} \over m_{kuru \ numune}} \times 100\]
\[ Yüzde \ kül= { 0,1006 \over 1,094} \times 100=9,2\]
Buradan sabit karbonu hesaplayacak olursak
\[ m_{sabit \ karbon}= m_{kok} - m_{kül}= 0,7767-0,1006 g=0,6761 \ g\]
\[ Yüzde \ sabit \ karbon= { m_{sabit \ karbon} \over m_{kuru \ numune}} \times 100\]
\[ Yüzde \ sabit \ karbon= { 0,6761 \over 1,094} \times 100=61,8\]
soruyu tamamlamış oluruz.




