Ölçme konusunda hatırlayacağınız gibi (Ölçme makalesine ulaşmak için lütfen tıklayınız) yapılan her ölçüm belirli seviyede belirsizlik içermektedir. Ölçüm cihazlarının kapasite ve hassasiyetleri arttıkça belirsizlik azalmakta olsa da sıfır belirsizlik mümkün değildir. Bu konuda sizlere endüstriyel analizler kapsamında yapılan titrasyon analizleri için örnek bir ölçüm belirsizliği tablosu hazırlama basamakları açıklanacaktır. Makale, Mettler Toledo firması tarafından hazırlanan "Bir titrasyon örneği için ölçüm belirsizliği hesaplama" adlı çalışmanın genel değerlendirmesi şeklinde olup orijinal metne buradaki linkten ulaşabilirsiniz.
Çalışma NaOH çözeltisinin primer standart potasyum hidrojen ftalat ile ayarlanması konusunda olup tüm basamakları detaylı açıklanmıştır
Genel olarak bir kimyasal analizde belirlenen sonuçların ölçüm belirsizliğini hesaplama prosedürü şu dört adımı içerir:
Adım 1: Ölçülen büyüklüğün belirlenmesi
Adım 2: İlgili tüm belirsizlik kaynaklarının belirlenmesi
Adım 3: Farklı belirsizlik bileşenlerinin ölçülmesi
Adım 4: Birleşik ölçüm belirsizliğinin hesaplanması
Bir titrasyon için pratikte bu dört adımın uygulanması, konsantrasyonun belirlenmesi için model olarak seçilmiştir potasyum hidrojen ftalat (KPH) primer standardı kullanılarak yeni hazırlanmış sodyum hidroksit (NaOH) çözeltisinin konsantrasyonunun nasıl belirleneceği açıklanmıştır. Örnek çalışma bir otomatik titratör kullanılarak gerçekleştirilmiş olup titrasyon sürecinde pH değişimi bir elektronik potansiyometre ile takip edilmiştir. Ancak burada uygulamayı yaş analiz yöntemi ile büret ve indikatör eşliğinde NaOH konsantrasyonu belirlenmesi için laboratuvar uygulaması şeklinde inceleyeceğiz. Titrasyon çalışması sonucunda NaOH çözeltisinin derişiminin yaklaşık 0.1 mol/L olduğu belirlenmiştir.
Adım 1 – Ölçülen Büyüklüğü Belirleme
Bu ilk adım da, laboratuvarda standart işletim prosedürlerine uygun şekilde titrasyon prosedürünün gerçekleştirilmesi amaçlanmaktadır. Analitik prosedürlerin bireysel adımlarını ve ölçülen büyüklüğün denklemini, eşdeğerlik noktasına kadar NaOH tüketimi gibi doğrudan bağlı olduğu tüm değişkenler ve parametrelerle açıklanır.
Laboratuvar föyüne benzer şekilde firma tarafından hazırlanan standart prosedür aşağıda verilmiştir.
1. KHP, tedarikçinin talimatlarına göre kurutulur ve bir numune, 0.1 mg çözünürlükte bir analitik terazide tartılır.
2. Çözeltinin CO2 içermediğinden emin olmak için gerekli tüm önlemler alınarak1 yaklaşık 0,1 mol/L NaOH'lik yeni bir çözelti hazırlanır.
3. Tartılan KHP numunesi yaklaşık 50 mL deiyonize suda çözülür ve ardından NaOH çözeltisi ile titre edilir. Sodyum hidroksit tüketimi indikatör çözeltisinin renk değiştirdiği noktadaki titrant hacmine göre belirlenir.
Yeni hazırlanmış bir sodyum hidroksit çözeltisinin derişimi aşağıdaki formülle hesaplanır:
Yukarıdaki formülde;
pKHP: potasyum hidrojen ftalat bileşiğinin saflığı
mKHP: potasyum hidrojen ftalat örneğinin kütlesi
Vdön: Dönüm noktasına kadar harcanan NaOH hacmi, mL
MAKHP: potasyum hidrojen ftalat bielşiğinin molekül kütlesini
ifade etmektedir.
Adım 2 – İlgili Tüm Belirsizlik Kaynaklarının Belirlenmesi
İkinci adımın amacı, tüm ana belirsizlik kaynaklarını belirlemek ve bunların ölçülen büyüklüğün ölçüm belirsizliği üzerindeki etkilerini anlamaktır. Bu aşamada, bir yandan önemli belirsizlik kaynaklarını ihmal etme, öte yandan diğer etkileri iki katına çıkarma riski olduğundan, ölçüm sonucunun belirsizliğini değerlendirmede en zor adımlardan biri olduğu düşünülebilir. Bir neden-sonuç diyagramının kullanılması, bu sorunların üstesinden gelmenin iyi bir yoludur. Diyagramı hazırlamanın ilk adımı, ölçülen büyüklük denkleminin dört parametresini ana dallar olarak çizmektir. Daha sonra, analitik prosedürün her adımı daha yakından incelenir ve bir parametre veya ölçülen büyüklük üzerindeki diğer etki faktörleri şemaya girilir. Bu, etkiler o kadar önemsiz olana ve sonuç üzerindeki etkileri ve belirsizliği ihmal edilebilir olana kadar her dal boyunca dışa doğru gerçekleştirilir. Aşağıda çalışma için örnek bir diyagram (balık kılçığı diyagramı da denir) sunulmuştur.
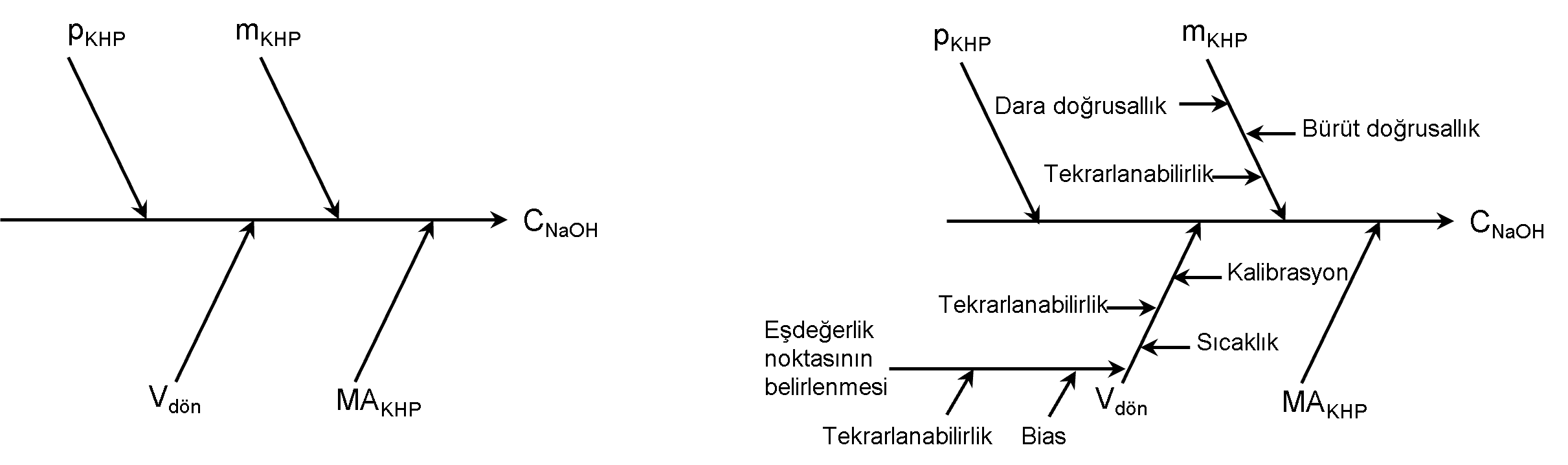
Bileşenleri inceleyecek olursak:
KHP primer standardının2 saflığı (pKHP), tedarikçinin kataloğunda %99,9 ve %100,1 sınırları içinde olacak şekilde belirtilmiştir. Primer standart, tedarikçinin spesifikasyonlarına göre kurutulursa, başka bir belirsizlik kaynağı yoktur.
KHP standardının kütlesi fark tartımı ile belirlenir. Boş beher önce dara ağırlığını belirlemek için teraziye yerleştirilir. Daha sonra primer standart behere eklenir ve ardından brüt ağırlık ölçülür. Her iki ölçüm için de, terazi tarafından kaydedilen kütle ile terazi üzerindeki gerçek kütle arasındaki olası fark, bir belirsizlik kaynağı olarak dikkate alınmalıdır. Bu fark, üretici tarafından doğrusallık olarak adlandırılır. Ağırlık farkı için sadece bir tekrarlanabilirlik belirlenebilir. Bu üç etki faktörü, sebep ve sonuç diyagramında belirsizlik kaynakları olarak girilir.
KHP'nin molar kütlesindeki belirsizlik, bileşiği oluşturan elementlerin atomik kütlelerindeki belirsizlik birleştirilerek belirlenebilir. Bu belirsizlik katkısı, diğer tüm belirsizlik kaynaklarına kıyasla önemsizdir ve konunun kapsamının dışındadır.
Eşdeğerlik noktasına kadar NaOH tüketimi için belirsizlik kaynakları iki gruba ayrılabilir. Birinci grup, NaOH çözeltisinin hacimsel olarak eklenmesiyle ilgili olan faktörlerini içerir. Cam büretinin kalibrasyonunu, iletilen hacmin tekrarlanabilirliği ve laboratuvardaki sıcaklık ile büretinin kalibre edildiği sıcaklık arasındaki farkın etkisini içerir. İkinci grup, analiz esnasında eşdeğerlik noktasının belirlenmesinde ve tekrarlanabilirliğinde sistematik bir fark veya bias3 ile ilgilidir.
Son olarak, yeni bir belirsizlik kaynağına birleştirilebilecek etki faktörlerini belirlemek için sebep ve sonuç diyagramı incelenir. Bu örnekte, yalnızca farklı parametrelerin tekrarlanabilirlik katkıları vardır. Katkılar, genel titrasyon için bir tekrarlanabilirlik katkısında birleştirilir ve diyagramda yeni bir ana dal olarak girilir.
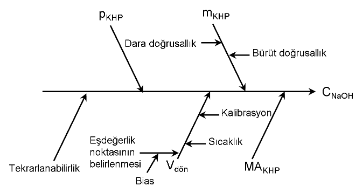
Bu şekilde bir neden-sonuç diyagramı oluşturularak belirsizlik kaynakları açıklanmış olacaktır. Konunun daha detaylı incelenmesi için örnek bir hesaplama çizelgesi yayınlanacaktır.
1 Bu uygulama yönergesinde titratör haznesi argon ile süpürülmekte ve hazne içerisine hava dolayısıyla karbon dioksit girişi engellenmektedir. Çünkü sulu çözeltisinde asidik özellikteki CO2 ile NaOH tepkimeye girecek olup NaOH derişiminin hazırlanan değerden farklı olmasına sebep olacaktır.
2 Primer standart tartımı alınarak doğrudan ayarlı çözeltisi hazırlanabilen kimyasallardır.
3 Analiz sonuçları (ölçülen değer) ile kabul edilen referans değer (gerçek değer) arasındaki farktır.
